Règles du forum
A LIRE AVANT DE POSER UNE QUESTION.- Pour créer un sujet ne pas écrire en majuscule faire un titre simple , soyez clair et précis , Contrôler les fautes d’orthographes.
- Si votre question concerne le KH ou les taux de Ca ou Mg indiquez aussi la densité ou la salinité.
- Si votre question concerne le système Balling indiquez aussi le Kh, les taux de Ca et Mg et la densité ou la salinité.
- Si vous mentionnez la densité ou la salinité indiquez aussi le moyen que vous utilisez pour la mesurer (réfractomètre, aréomètre, ...).
- Indiquez la marque des tests et, pour le Kh et le pH, l'heure par rapport à la photopériode (juste après allumage de l'éclairage, juste avant l'extinction, ...).
Re: Balling base carbonate ( explications)
Ven 23 Mar 2018, 21:51
Morlock a écrit:Je trouve que la méthode Fauna Marin n'est pas plus ou moins compliquée mais elle est plus flexible, quand le rythme est prit il suffit de suivre les analyses Kh Ca (et Mg) et d'augmenter les doses indépendamment les unes des autres par les pompes doseuses dédiées, choisir la valeur Ca souhaitée par la valeur Kh souhaitée.
Tu peux faire exactement la même chose avec un balling classique, il suffit de savoir que le "sel sans NaCl" est constitué essentiellement de Mg.
Chez moi en 2 ans, j'ai toujours versé 3 doses identiques ; et j'ai dû corriger une fois le Ca et 2 fois le Mg : l'équilibre des doses est quasi parfait.
Re: Balling base carbonate ( explications)
Ven 23 Mar 2018, 22:22
Je n'ai pas compris ton message og, Mg dans le sel sans sel sous quelle forme MgCl2 ou MgSO4 ?
Sinon, dans la méthode classique d''après ce que j'ai compris tu mets ma même dose de chaque produit, donc tu ne peux ps ajuster spécifiquement un paramètre. Tu dis que c'est possible c'est ca ?
Sinon, dans la méthode classique d''après ce que j'ai compris tu mets ma même dose de chaque produit, donc tu ne peux ps ajuster spécifiquement un paramètre. Tu dis que c'est possible c'est ca ?
Re: Balling base carbonate ( explications)
Ven 23 Mar 2018, 22:56
lirone a écrit:Je n'ai pas compris ton message og, Mg dans le sel sans sel sous quelle forme MgCl2 ou MgSO4 ?
C'est un mélange de ces 2 produits dans les bonnes proportions pour respecter l'équilibre ionique. Il y a aussi quelques autres produits dans ce sel minéral, mais en faible quantité.
lirone a écrit:Sinon, dans la méthode classique d''après ce que j'ai compris tu mets ma même dose de chaque produit, donc tu ne peux ps ajuster spécifiquement un paramètre. Tu dis que c'est possible c'est ca ?
C'est plus simple de verser 3 doses identiques, et ça convient parfaitement ou presque parfaitement pour la plupart des aquariums. Si ça ne te convient pas, aucune loi ne t'interdit d'ajuster chaque dose. Je dis seulement que ça n'est pas logique de verser des doses très différentes, normalement les coraux consomment le calcium et le KH dans les proportions prévues par la méthode balling. Cette remarque est tout aussi vraie pour la méthode Fauna Marin.
Re: Balling base carbonate ( explications)
Ven 23 Mar 2018, 23:06
Ce que je comprends pas c'est comment MgCl2 et MgSO4 respectent totalement la balance ionique, car ca donne 2 Cl- et 1 SO4-- ca apporte donc des sulfates mais par contre ca crée un déficit en Na+.
Après sur les proportions, si tu me dis que c'est bien "calibré", je te crois c'est ce que je demandais sans arrière-pensée (je suis juste échaudé par le produit red sea complete reef fundation, avec lequel le KH a tendance à chuter par rapport au Ca).
Après sur les proportions, si tu me dis que c'est bien "calibré", je te crois c'est ce que je demandais sans arrière-pensée (je suis juste échaudé par le produit red sea complete reef fundation, avec lequel le KH a tendance à chuter par rapport au Ca).
Modifié en dernier par lirone le Ven 23 Mar 2018, 23:10, modifié 1 fois.
Re: Balling base carbonate ( explications)
Ven 23 Mar 2018, 23:08
Au niveau ionique qu’est ce que ça change d’avoir 2 ions Cl- avec du chlorure de Mg ou 1 ion SO42- avec du sulfate de Mg ?
Perso je préfère faire 3 tests des 3 paramètres que je veux remonter et administrer ce que mon bac consomme sans me soucier du reste, chacun son truc ;)
Édit : pour l’histoire des ions lirone m’a devancé ^^ les ions Na+ sont apporté par le (bi)carbonate de sodium
Perso je préfère faire 3 tests des 3 paramètres que je veux remonter et administrer ce que mon bac consomme sans me soucier du reste, chacun son truc ;)
Édit : pour l’histoire des ions lirone m’a devancé ^^ les ions Na+ sont apporté par le (bi)carbonate de sodium
Re: Balling base carbonate ( explications)
Ven 23 Mar 2018, 23:14
Hemix a écrit:Édit : pour l’histoire des ions lirone m’a devancé ^^ les ions Na+ sont apporté par le (bi)carbonate de sodium
Ces ions ne sont-ils déjà compensés par les Cl- du chlorure de calcium issus de CA1 ?
Re: Balling base carbonate ( explications)
Ven 23 Mar 2018, 23:29
Hemix a écrit:Au niveau ionique qu’est ce que ça change d’avoir 2 ions Cl- avec du chlorure de Mg ou 1 ion SO42- avec du sulfate de Mg ?
Rien à mon avis. Ce n'est pas, je pense, pour cela qu'on dit que ca équilibre la balance ionique.
voir :
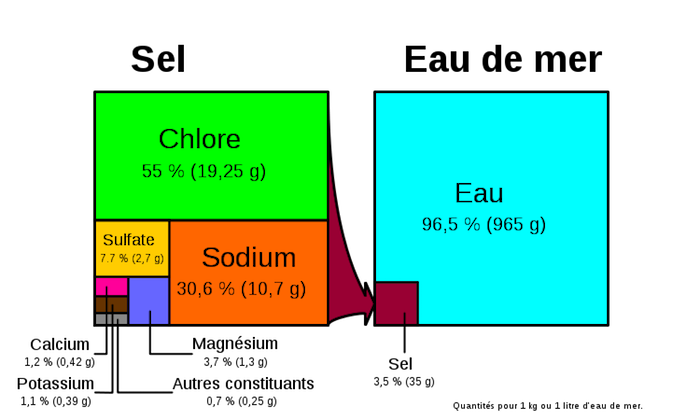
On voit qu'il y a une bonne quantité de sulfate dans l'eau, c'est pourquoi c'est bien d'ajouter les deux dans les bonnes proportions. Mais je reste dans l'expectative sur le sodium qui manque dans l'apport.
Re: Balling base carbonate ( explications)
Ven 23 Mar 2018, 23:39
lirone a écrit:Ce que je comprends pas c'est comment MgCl2 et MgSO4 respectent totalement la balance ionique, car ca donne 2 Cl- et 1 SO4-- ca apporte donc des sulfates mais par contre ca crée un déficit en Na+.
Après sur les proportions, si tu me dis que c'est bien "calibré", je te crois c'est ce que je demandais sans arrière-pensée (je suis juste échaudé par le produit red sea complete reef fundation, avec lequel le KH a tendance à chuter par rapport au Ca).
C'est l'ensemble de la méthode balling avec les 3 doses identiques qui arrive à un équilibre ionique. Ou plutôt à une augmentation générale de la salinité, c'est pourquoi il faut retirer un peu d'eau de temps en temps et la remplacer par de l'eau osmosée, sinon la salinité augmente.
Les ions SO4 ne sont pas consommés dans l'aquarium, mais le jour où on va retirer de l'eau pour baisser la salinité, on va retirer des SO4 : donc la méthode balling en ajoute, pour compenser leur retrait ultérieur.
Pareil pour les autres produits : les apports de Na avec les carbonates et de Cl avec le magnésium et le calcium seront retirés quand on jettera un peu d'eau pour baisser la salinité. Etc etc etc ...
Les méthodes avec 2 produits, ou 2 produits + Mg ne peuvent pas respecter totalement cette balance ionique, c'est chimiquement impossible. Ces méthodes partent avec un handicap dès leur conception, qui ne pourra être compensé que par les changements d'eau. La vraie méthode balling est chimiquement parfaite. Si on verse des doses différentes, on s'écarte de la perfection, on crée de petits déséquilibres, c'est moins bien mais ça n'est pas non-plus dramatique.
Re: Balling base carbonate ( explications)
Ven 23 Mar 2018, 23:42
lirone a écrit: Mais je reste dans l'expectative sur le sodium qui manque dans l'apport.
les carbonates et/ou bicarbonates de sodium sont là pour ça

Re: Balling base carbonate ( explications)
Ven 23 Mar 2018, 23:43
og a écrit:lirone a écrit:Ce que je comprends pas c'est comment MgCl2 et MgSO4 respectent totalement la balance ionique, car ca donne 2 Cl- et 1 SO4-- ca apporte donc des sulfates mais par contre ca crée un déficit en Na+.
Après sur les proportions, si tu me dis que c'est bien "calibré", je te crois c'est ce que je demandais sans arrière-pensée (je suis juste échaudé par le produit red sea complete reef fundation, avec lequel le KH a tendance à chuter par rapport au Ca).
C'est l'ensemble de la méthode balling avec les 3 doses identiques qui arrive à un équilibre ionique.
ok là je comprends mieux.
Re: Balling base carbonate ( explications)
Ven 23 Mar 2018, 23:47
C’est je pense pour ça que le Magnesium mix de FM n’apporte que du chlorure de Mg, et pas de sulfate, pour éviter une accumulation en cas de changement d’eau insuffisant
Re: Balling base carbonate ( explications)
Sam 24 Mar 2018, 08:12
Hemix a écrit:C’est je pense pour ça que le Magnesium mix de FM n’apporte que du chlorure de Mg, et pas de sulfate, pour éviter une accumulation en cas de changement d’eau insuffisant
On fait 2 choses dans un aquarium sous balling :
- des "changements d'eau" = j'enlève de l'eau salée et je remets la même quantité d'eau salée neuve = je retire des sulfates et j'en remets aussitôt la même quantité : bilan = 0
- des opérations de "diminution de salinité" = j'enlève de l'eau salée et je remets la même quantité d'eau osmosée. Ces opérations sont nécessaires parce que le balling augmente la salinité de l'eau de l'aquarium. C'est à cette occasion que l'on retire les sulfates qui se sont accumulés, ainsi que les chlorures, les sodiums, etc.
La méthode balling a augmenté la salinité en augmentant la concentration de tous les ions dans les mêmes proportions que dans l'eau de mer naturelle. Donc en retirant un peu d'eau salée, on retire exactement ce qu'il faut de chaque ion, notamment les sulfates, pour retrouver une eau à la bonne salinité et avec un équilibre ionique parfait.
Bref, une méthode balling sans sulfate, c'est très curieux, ça crée obligatoirement un déséquilibre ionique.
Re: Balling base carbonate ( explications)
Sam 24 Mar 2018, 11:25
Je ne suis pas d’accord : si il y a accumulation de sulfates par le biais du balling, lors d’un changement d’eau classique on va enlever de l’eau surchargé en cet ion pour la remplacer par de l’eau neuve qui en contient, mais en proportion normale donc on en retire bien.
Après les proportions des différents ions par rapport à l’eau de mer naturelle, et la balance ionique sont à mes yeux 2 concepts distincts (je me trompe peut être).
Comme je l’ai déjà dit, au niveau des valences je ne vois pas la différence entre 2 ions chlorure et 1 ion sulfate, donc pour moi la balance ionique est respectée.
Sachant qu’a mes yeux, après avoir lu pas mal de chose en Allemagne ou aux usa, la balance ionique c’est un concept dont a peu prêt seuls les français se pré-occupent de part le monde au niveau Récifal, et pourtant on est pas les plus en avance ...
Après les proportions des différents ions par rapport à l’eau de mer naturelle, et la balance ionique sont à mes yeux 2 concepts distincts (je me trompe peut être).
Comme je l’ai déjà dit, au niveau des valences je ne vois pas la différence entre 2 ions chlorure et 1 ion sulfate, donc pour moi la balance ionique est respectée.
Sachant qu’a mes yeux, après avoir lu pas mal de chose en Allemagne ou aux usa, la balance ionique c’est un concept dont a peu prêt seuls les français se pré-occupent de part le monde au niveau Récifal, et pourtant on est pas les plus en avance ...
Re: Balling base carbonate ( explications)
Sam 24 Mar 2018, 12:23
Hemix a écrit:Je ne suis pas d’accord : si il y a accumulation de sulfates par le biais du balling
Oui le balling accumule des sulfates ; et des chlorures, et des sodiums, etc. Globalement il accumule du sel marin, c'est la salinité qui augmente en gardant les mêmes proportions que dans l'eau de mer naturelle.
Bien sûr on peut rétablir la salinité en faisant énormément de changements d'eau ; mais c'est infiniment plus rapide en retirant un peu d'eau et en la remplaçant par de l'eau osmosée

Nous n'avons pas la même définition de la "balance ionique". Il ne s'agit pas de vérifier qu'il y a autant d'ions + et d'ions - : c'est toujours le cas, même dans une batterie électrique ! Il s'agit de vérifier que chaque ion se trouve dans l'eau de l'aquarium dans les mêmes proportions que dans l'eau de mer naturelle.
Par exemple (je prends des chiffres au hasard), s'il y a 10 fois plus de sodium que de sulfates dans l'eau de mer naturelle, ça doit être pareil dans l'aquarium. La méthode balling respecte parfaitement cet équilibre.
Re: Balling base carbonate ( explications)
Dim 25 Mar 2018, 16:18
Je ne suis pas assez assidu sur le forum ... il y a des supers sujets que je loupe.
Celui-ci en particulier.
Pour ma part, je suis en balling classique, et je ne m'embête même pas à enlever de l'eau salée : quand je fais des changements d'eau, je calcule la salinité de mon eau "propre" en fonction de la salinité du bac : le résultat combiné doit tomber à 35.
Exemple :
Je mesure 36 de salinité dans mon bac de 400L. Je veux changer 10% : je prépare 40L d'eau neuve, il restera 360L d'eau dans le bac. Mon eau "propre", je ne la mets pas à 35 de salinité... en fait, je la mets à 26 !
Du coup, après changement, ma salinité sera de (360*36 + 40*26) / (360+40) = 35.
Le compte est bon.
Ca me permet de ne pas me prendre la tête, et d'économiser du sel...
A part ca, je viens de voir que je pouvais tripler mon autonomie : génial !!
La seule question qui me reste, c'est que chez Tridacna, on peut mélanger les oligo éléments directement dans les bidons de balling. Est-ce qu'on peut tripler la concentration des oligo éléments, dans une base carbonate triple, sans précipitation ? (j'ai mal vu/compris la réponse).
Celui-ci en particulier.
Pour ma part, je suis en balling classique, et je ne m'embête même pas à enlever de l'eau salée : quand je fais des changements d'eau, je calcule la salinité de mon eau "propre" en fonction de la salinité du bac : le résultat combiné doit tomber à 35.
Exemple :
Je mesure 36 de salinité dans mon bac de 400L. Je veux changer 10% : je prépare 40L d'eau neuve, il restera 360L d'eau dans le bac. Mon eau "propre", je ne la mets pas à 35 de salinité... en fait, je la mets à 26 !
Du coup, après changement, ma salinité sera de (360*36 + 40*26) / (360+40) = 35.
Le compte est bon.
Ca me permet de ne pas me prendre la tête, et d'économiser du sel...
A part ca, je viens de voir que je pouvais tripler mon autonomie : génial !!
La seule question qui me reste, c'est que chez Tridacna, on peut mélanger les oligo éléments directement dans les bidons de balling. Est-ce qu'on peut tripler la concentration des oligo éléments, dans une base carbonate triple, sans précipitation ? (j'ai mal vu/compris la réponse).
Re: Balling base carbonate ( explications)
Dim 25 Mar 2018, 17:06
Jérôme a écrit:...
La seule question qui me reste, c'est que chez Tridacna, on peut mélanger les oligo éléments directement dans les bidons de balling. Est-ce qu'on peut tripler la concentration des oligo éléments, dans une base carbonate triple, sans précipitation ? (j'ai mal vu/compris la réponse).
Je n’en suis pas mais je ne penses pas.
Si tu dois mettre des choses dans le Ca2, le carbonate de sodium ayant un pH élevé, il y a des chances que ça ineragisse.
Tu peux faire l’essais et voir si quelque chose précipite.
Re: Balling base carbonate ( explications)
Dim 25 Mar 2018, 17:14
Ou poser la question a ton fournisseur de balling si ce n’est pas juste un revendeur ;)
Re: Balling base carbonate ( explications)
Dim 25 Mar 2018, 17:23
Je me fournis chez Tridacna ... je dois avoir 4 ou 5 recharges de 5L d'avance.
J'ai donc le temps de voir venir ! Je lui poserai la question à l'occasion (il faudra par contre que je me passe de lui pour le sel sans NaCl pour des raisons de dissolution, si j'ai bien compris).
Si vous utilisez des pompes doseuses à part, vous mettez quelles doses en oligo du coup (strontium, bode, iode, etc ...) ?
C'est basé sur la concentration de Ca / KH ?
J'ai donc le temps de voir venir ! Je lui poserai la question à l'occasion (il faudra par contre que je me passe de lui pour le sel sans NaCl pour des raisons de dissolution, si j'ai bien compris).
Si vous utilisez des pompes doseuses à part, vous mettez quelles doses en oligo du coup (strontium, bode, iode, etc ...) ?
C'est basé sur la concentration de Ca / KH ?
Re: Balling base carbonate ( explications)
Dim 25 Mar 2018, 18:16
Oui les besoins en oligos sont proportionnels aux besoins Ca et KH.
La formule est secrète et à ne divulguer sous aucun prétexte .
.
La voici :
:
Pour des bidons de 5L de balling en concentration classique (tridacna, aquafair, etc), il faut ajouter 25mL de chaque solution d'oligos, et ces 25 mL contiennent les produits suivants :
- Sr = 2 g
- Ba = 5 mg
- I = 47.5 mg
- F = 139 mg
- B = 10 mg
Je vous épargne la liste des métaux, il faudrait être fou pour vouloir les doser un par un !
Les chlorures de strontium et de baryum peuvent être mélangés ensemble = une pompe doseuse
Les iodure de potassium, fluorure de sodium et borate de sodium peuvent être mélangés ensemble = une autre pompe doseuse
La formule est secrète et à ne divulguer sous aucun prétexte
 .
.La voici
 :
:Pour des bidons de 5L de balling en concentration classique (tridacna, aquafair, etc), il faut ajouter 25mL de chaque solution d'oligos, et ces 25 mL contiennent les produits suivants :
- Sr = 2 g
- Ba = 5 mg
- I = 47.5 mg
- F = 139 mg
- B = 10 mg
Je vous épargne la liste des métaux, il faudrait être fou pour vouloir les doser un par un !

Les chlorures de strontium et de baryum peuvent être mélangés ensemble = une pompe doseuse
Les iodure de potassium, fluorure de sodium et borate de sodium peuvent être mélangés ensemble = une autre pompe doseuse