Règles du forum
A LIRE AVANT DE POSER UNE QUESTION.
- Pour créer un sujet ne pas écrire en majuscule faire un titre simple , soyez clair et précis , Contrôler les fautes d’orthographes.
- Si votre question concerne le KH ou les taux de Ca ou Mg indiquez aussi la densité ou la salinité.
- Si votre question concerne le système Balling indiquez aussi le Kh, les taux de Ca et Mg et la densité ou la salinité.
- Si vous mentionnez la densité ou la salinité indiquez aussi le moyen que vous utilisez pour la mesurer (réfractomètre, aréomètre, ...).
- Indiquez la marque des tests et, pour le Kh et le pH, l'heure par rapport à la photopériode (juste après allumage de l'éclairage, juste avant l'extinction, ...).
A LIRE AVANT DE POSER UNE QUESTION.
- Pour créer un sujet ne pas écrire en majuscule faire un titre simple , soyez clair et précis , Contrôler les fautes d’orthographes.
- Si votre question concerne le KH ou les taux de Ca ou Mg indiquez aussi la densité ou la salinité.
- Si votre question concerne le système Balling indiquez aussi le Kh, les taux de Ca et Mg et la densité ou la salinité.
- Si vous mentionnez la densité ou la salinité indiquez aussi le moyen que vous utilisez pour la mesurer (réfractomètre, aréomètre, ...).
- Indiquez la marque des tests et, pour le Kh et le pH, l'heure par rapport à la photopériode (juste après allumage de l'éclairage, juste avant l'extinction, ...).
Compléments Balling + RAC
Bonsoir ,
J'ai entendu parler que certain récifaliste combinait à la fois le RAC et le Balling.
Y a t'il des personnes qui utilise cette méthode ? comment faite vous ? avantage ?
J'ai entendu parler que certain récifaliste combinait à la fois le RAC et le Balling.
Y a t'il des personnes qui utilise cette méthode ? comment faite vous ? avantage ?
- alain.se

-

- Messages: 2192
- Âge: 56 ans
- Enregistré le: 29/04/2012
- Localisation: noyon
- volume du bac: Xénia130+refuge
- maintenance: berlinois
- éclairage: 2 GIESEMANN Vervve
- mon bac: alain-se-2eme-version-c-est-parti-t32884.html
Re: Compléments Balling + RAC
En principe le Balling se compose de 3 solutions : calcium, carbonates (KH) et le reste (magnésium, oligo, ...).
Le RAC fournit calcium et carbonates ainsi que, si on choisit bien son substrat, magnésium et strontium.
Je ne vois donc pas l'intérêt de combiner les 2, la seule différence étant que le Balling apporte aussi des oligo-éléments : un RAC apporte tout ce dont le bac a besoin, les changements d'eau apportent les oligos.
Le RAC fournit calcium et carbonates ainsi que, si on choisit bien son substrat, magnésium et strontium.
Je ne vois donc pas l'intérêt de combiner les 2, la seule différence étant que le Balling apporte aussi des oligo-éléments : un RAC apporte tout ce dont le bac a besoin, les changements d'eau apportent les oligos.
_____________________________
... ce que j'écris n'est jamais que mon avis.
... ce que j'écris n'est jamais que mon avis.
- Hervé

- Messages: 18709
- Âge: 72 ans
- Enregistré le: 21/06/2011
- Localisation: Jurbise - Belgique
- volume du bac: 750
- mise en eau: 03/07/2004
- maintenance: berlinois
- éclairage: LED DIY
Re: Compléments Balling + RAC
Donc aucun intérêt à par se prendre la tête ?
- alain.se

-

- Messages: 2192
- Âge: 56 ans
- Enregistré le: 29/04/2012
- Localisation: noyon
- volume du bac: Xénia130+refuge
- maintenance: berlinois
- éclairage: 2 GIESEMANN Vervve
- mon bac: alain-se-2eme-version-c-est-parti-t32884.html
Re: Compléments Balling + RAC
A mon avis, non.alain.se a écrit:Donc aucun intérêt à par se prendre la tête ?
Je vais faire mon relou mais c'est "à part"

_____________________________
... ce que j'écris n'est jamais que mon avis.
... ce que j'écris n'est jamais que mon avis.
- Hervé

- Messages: 18709
- Âge: 72 ans
- Enregistré le: 21/06/2011
- Localisation: Jurbise - Belgique
- volume du bac: 750
- mise en eau: 03/07/2004
- maintenance: berlinois
- éclairage: LED DIY
Re: Compléments Balling + RAC
Hervé a écrit:A mon avis, non.alain.se a écrit:Donc aucun intérêt à par se prendre la tête ?
Je vais faire mon relou mais c'est "à part"
 bien vu , mais c'était juste pour remonter le tuto en Haut ! ! !
bien vu , mais c'était juste pour remonter le tuto en Haut ! ! ! 
Et ce n'est pas le même appareil !
- alain.se

-

- Messages: 2192
- Âge: 56 ans
- Enregistré le: 29/04/2012
- Localisation: noyon
- volume du bac: Xénia130+refuge
- maintenance: berlinois
- éclairage: 2 GIESEMANN Vervve
- mon bac: alain-se-2eme-version-c-est-parti-t32884.html
Re: Compléments Balling + RAC
Hervé a écrit:En principe le Balling se compose de 3 solutions : calcium, carbonates (KH) et le reste (magnésium, oligo, ...).
Le RAC fournit calcium et carbonates ainsi que, si on choisit bien son substrat, magnésium et strontium.
Je ne vois donc pas l'intérêt de combiner les 2, la seule différence étant que le Balling apporte aussi des oligo-éléments : un RAC apporte tout ce dont le bac a besoin, les changements d'eau apportent les oligos.
En balling simple ou carbonate (zoanthus, Tridacna, ...), à ma connaissance les oligo ne sont pas présents dans les 3 solutions (Chlorure de calcium, bicarbonate ou carbonate de sodium, sel sans sel). Ils sont généralement vendus à part et leurs ajouts doivent être bien cadrés car il n'est pas possible de les tester hormis les tests ICP.
Dans le cas d'un RAC sous dimensionné par rapport à la conso du bac, combiner les 2 peut permettre d'apporter via les pompes doseuses le complément que le RAC n'est pas en capacité d'apporter.
Mais sous réserve d'en avoir la place, il est peut-être plus simple de passer à un RAC d'une capacité supérieure.
Ou d'être uniquement en balling ... Quant la conso augmente, il suffit d'augmenter les doses distribuées quotidiennement.
- yaya

-

- Messages: 2350
- Âge: 55 ans
- Enregistré le: 16/10/2014
- Localisation: 91620
- volume du bac: 1800 litres bruts
- mise en eau: 12/2021
- maintenance: berlinois
- éclairage: AI HYDRA 64hd
- mon bac: la-nouvelle-bassine-de-yaya-t41536.html?sid=29b481352dfa5a89200f5a0fd6d
Re: Compléments Balling + RAC
Je suis d'accord avec ce que tu écris sauf que je persiste à croire qu'il est compliqué de combiner RAC et Balling.
Quand à la dimension d'un RAC voici un graphique qui montre quel devrait être son volume en fonction de celui du système (bac + cuve technique), de la consommation KH du bac et du type de substrat.
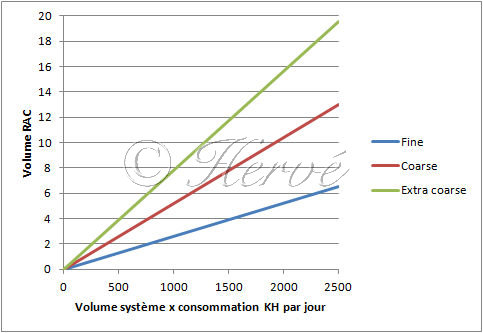
Quand à la dimension d'un RAC voici un graphique qui montre quel devrait être son volume en fonction de celui du système (bac + cuve technique), de la consommation KH du bac et du type de substrat.

_____________________________
... ce que j'écris n'est jamais que mon avis.
... ce que j'écris n'est jamais que mon avis.
- Hervé

- Messages: 18709
- Âge: 72 ans
- Enregistré le: 21/06/2011
- Localisation: Jurbise - Belgique
- volume du bac: 750
- mise en eau: 03/07/2004
- maintenance: berlinois
- éclairage: LED DIY
Re: Compléments Balling + RAC
Il est probablement plus intéressant de combiner le balling avec un RAH plutôt un RAC. Comme Hervé l'a déjà dit, pour moi le RAC est une alternative au balling.
Le RAH aura lui l'avantage de maintenir un PH haut contraitement au balling classique. L'hydrogénocarbonate de sodium du balling classique réagit en fonction du taux le co2 contenu dans l'eau, et forme soit de l'acide carbonique, soit des carbonates
Le RAH aura lui l'avantage de maintenir un PH haut contraitement au balling classique. L'hydrogénocarbonate de sodium du balling classique réagit en fonction du taux le co2 contenu dans l'eau, et forme soit de l'acide carbonique, soit des carbonates
- Space

- Messages: 2231
- Âge: 36 ans
- Enregistré le: 27/09/2017
- Localisation: Lyon
- volume du bac: 350L
- mise en eau: 16/11/2017
- maintenance: berlinois
- éclairage: Evergrow IT5080
- mon bac: reefer-350-de-space-t32720.html
Re: Compléments Balling + RAC
Space a écrit:le RAC est une alternative au balling
Et inversement.
- yaya

-

- Messages: 2350
- Âge: 55 ans
- Enregistré le: 16/10/2014
- Localisation: 91620
- volume du bac: 1800 litres bruts
- mise en eau: 12/2021
- maintenance: berlinois
- éclairage: AI HYDRA 64hd
- mon bac: la-nouvelle-bassine-de-yaya-t41536.html?sid=29b481352dfa5a89200f5a0fd6d
Re: Compléments Balling + RAC
yaya a écrit:En balling simple ou carbonate (zoanthus, Tridacna, ...), à ma connaissance les oligo ne sont pas présents dans les 3 solutions (Chlorure de calcium, bicarbonate ou carbonate de sodium, sel sans sel). Ils sont généralement vendus à part et leurs ajouts doivent être bien cadrés car il n'est pas possible de les tester hormis les tests ICP.
Pourtant les oligos sont fournis avec les SET Balling (a mélanger avec le Calcium et le Carbonate) ? non ?


- Phiphi7

-

- Messages: 7811
- Âge: 55 ans
- Enregistré le: 17/05/2018
- Localisation: Villiers sur Marne 94350
- volume du bac: 275+70+10
- mise en eau: le 01/07/2018
- maintenance: berlinois
- éclairage: 2 Coral Care Philips
- mon bac: 1 Reefer 350 DeLuxe
Re: Compléments Balling + RAC
Je pense qu'il vaut mieux ne pas combiner le Balling ni avec un RAC ni avec un RAH.Space a écrit:Il est probablement plus intéressant de combiner le balling avec un RAH plutôt un RAC.
Je ne vois pas comment l'hydrogénocarbonate NaHCO3 pourrait former de l'acide carbonique H2CO3 en présence de CO2; tu ne confoncdrais pas avec l'hydroxyde du RAH ?Space a écrit:L'hydrogénocarbonate de sodium du balling classique réagit en fonction du taux le co2 contenu dans l'eau, et forme soit de l'acide carbonique, soit des carbonates
Je pense que l'hydrogénocarbonate va former un couple HCO3- / CO3-- dont la proportion entre les deux dépendra du pH.
Ceci dit, je ne suis pas chimiste ...
_____________________________
... ce que j'écris n'est jamais que mon avis.
... ce que j'écris n'est jamais que mon avis.
- Hervé

- Messages: 18709
- Âge: 72 ans
- Enregistré le: 21/06/2011
- Localisation: Jurbise - Belgique
- volume du bac: 750
- mise en eau: 03/07/2004
- maintenance: berlinois
- éclairage: LED DIY
Re: Compléments Balling + RAC
Phiphi7 a écrit:Pourtant les oligos sont fournis avec les SET Balling (a mélanger avec le Calcium et le Carbonate) ? non ?
Fournis avec oui, quand tu achète le set balling.
Mais pas si tu prends chaque produit (Chlorure de calcium, bicarbonate ou carbonate de sodium, sel sans sel) individuellement.
Et dans le set balling ils sont vendus à part dans des bouteilles séparées. Les oligo ne sont donc pas présents dans les 3 solutions.
- yaya

-

- Messages: 2350
- Âge: 55 ans
- Enregistré le: 16/10/2014
- Localisation: 91620
- volume du bac: 1800 litres bruts
- mise en eau: 12/2021
- maintenance: berlinois
- éclairage: AI HYDRA 64hd
- mon bac: la-nouvelle-bassine-de-yaya-t41536.html?sid=29b481352dfa5a89200f5a0fd6d
Re: Compléments Balling + RAC
Hervé a écrit:Je ne vois pas comment l'hydrogénocarbonate NaHCO3 pourrait former de l'acide carbonique H2CO3 en présence de CO2; tu ne confoncdrais pas avec l'hydroxyde du RAH ?Space a écrit:L'hydrogénocarbonate de sodium du balling classique réagit en fonction du taux le co2 contenu dans l'eau, et forme soit de l'acide carbonique, soit des carbonates
Je pense que l'hydrogénocarbonate va former un couple HCO3- / CO3-- dont la proportion entre les deux dépendra du pH.
Ceci dit, je ne suis pas chimiste ...
J'ai repris ces infos ici: http://greg-aqua-hifi.monsite-orange.fr ... 3d87b.html
J'ai plus confiance en tes informations détaillées avec des formules que celle de ce lien. Du coup j'ai peut être cité des bêtises
- Space

- Messages: 2231
- Âge: 36 ans
- Enregistré le: 27/09/2017
- Localisation: Lyon
- volume du bac: 350L
- mise en eau: 16/11/2017
- maintenance: berlinois
- éclairage: Evergrow IT5080
- mon bac: reefer-350-de-space-t32720.html
Re: Compléments Balling + RAC
Si tu te réfères à ce passageSpace a écrit:J'ai repris ces infos ici: http://greg-aqua-hifi.monsite-orange.fr ... 3d87b.htmlHervé a écrit:Je ne vois pas comment l'hydrogénocarbonate NaHCO3 pourrait former de l'acide carbonique H2CO3 en présence de CO2; tu ne confoncdrais pas avec l'hydroxyde du RAH ?Space a écrit:L'hydrogénocarbonate de sodium du balling classique réagit en fonction du taux le co2 contenu dans l'eau, et forme soit de l'acide carbonique, soit des carbonates
Je pense que l'hydrogénocarbonate va former un couple HCO3- / CO3-- dont la proportion entre les deux dépendra du pH.
Ceci dit, je ne suis pas chimiste ...
J'ai plus confiance en tes informations détaillé avec des formules que celle de ce lien. Du coup j'ai peut être cité des bêtises
Le plus gros système tampon en eau de mer est constitué par le couple Carbonate (CO3--) /Hydrogénocarbonate (HCO3-).
Quand il y a beaucoup de Co2 dissous dans l'eau , qui forme de l’acide carbonique, c'est l'hydrogénocarbonate qui « domine", le PH est "bas".
Si la quantité de Co2 dissout baisse dans l’eau de l’aquarium, une partie de l'hydrogénocarbonate devient du carbonate, le PH monte.
C'est correct mais je pense que tu as mal interprété : ce n'est pas l'hydrogénocarbonate qui diminue le pH c'est le CO2.
Au contraire en fonction du pH la proportion entre HCO3- et CO3-- se modifie ce qui contre la variation de pH; en fait l'hydrogénocarbonate de sodium du balling classique va former un tampon qui stabilise le pH.
Du moins c'est ce que j'ai compris, je suis électronicien, pas chimiste.
_____________________________
... ce que j'écris n'est jamais que mon avis.
... ce que j'écris n'est jamais que mon avis.
- Hervé

- Messages: 18709
- Âge: 72 ans
- Enregistré le: 21/06/2011
- Localisation: Jurbise - Belgique
- volume du bac: 750
- mise en eau: 03/07/2004
- maintenance: berlinois
- éclairage: LED DIY
Re: Compléments Balling + RAC
Exacte. Merci pour l'explication. J'ai compris où était mon erreur d’interprétation
- Space

- Messages: 2231
- Âge: 36 ans
- Enregistré le: 27/09/2017
- Localisation: Lyon
- volume du bac: 350L
- mise en eau: 16/11/2017
- maintenance: berlinois
- éclairage: Evergrow IT5080
- mon bac: reefer-350-de-space-t32720.html
Re: Compléments Balling + RAC
Bonjour,
Je vais peut être faire un article un jour sur la comparaison des différents méthodes de complémentation de Ca et Kh.
dans le cadre de cette discussion il y a deux aspects de cette comparaison que je voudrais expliquer:
1- Apport d'autres éléments de Ca et Kh:
Des méthodes comme le RAC, en fonction du granulat qu'on met dans le RAC, va apporter potentiellement, en plus de Ca et Kh, d'autres macro et micro éléments comme Mg, et tous les oligos éléments. Typiquement quand on met de l'aragonite qui est du squelette de corail broyé, on redissout du squelette de corail donc on va apporter à peu près tout ce que la pousse des coraux consomme.
Ceci est un peu moins vrai pour les méthodes bailing qui respectent bien l'équilibre ionique de l'eau mais qui ne vont apporter potentiellement tout le Mg et oligos que les coraux ont consommés.
Et enfin, dans les méthodes basée sur l'hydroxyde de calcium, ceci est complètement réduit à zéro: l'hydroxyde de calcium n'apporte que du Ca et du Kh (en devenir). Et donc rien d'autre. Pas de Mg, strontium, oligos,...
2- Influence sur le Ph:
chacun de ces méthodes de complémentation va influencer plus ou moins le Ph et sachant l'importance du Ph dans la pousse des coraux, suivant comment le bac se comporte en ph, ce point peut être un élément de décision important pour savoir quelle méthode de complémentation choisir:
Un bac surpeuplé où on est obligé d'avoir recours à une source de carbone pour contrôler les nitrates et phosphates, aura tendance à avoir un ph trop bas. Et donc une méthode de complémentation qui monte le ph sera plus adaptée.
Maintenant comparons les différentes méthodes de complémentation de ce point de vue:
RAC:
Le RAc, bien dimensionné et bien réglé, va rejeter peu de CO2 dans le bac. Donc si on utilise bien le RAC, le RAC est neutre point de vue Ph.
Bailing classique:
Le Bailing classique à base de bicarbonate de sodium est aussi neutre point de vue Ph. Donc disons que c'est légèrement mieux que le RAC mais la différence est faible dans le cas d'un RAC bien dimensionné et bien réglé.
Bailing base carbonate:
Le Bailing base carbonate, remplace le bicarbonate de sodium par du carbonate de sodium.
Pour pas rentrer dans des formules chimiques (ça me démange! ), en vue simplifiée, chaque molécule de carbonate sodium par rapport à un molécule de bicarbonate de sodium, est en manque d'un molécule de CO2 dissout dans le bac. Donc va en arrivant dans le bac chercher à absorber le CO2 dissout. C'est ça qui va aider le bac à monter en Ph. Plus le bac est consommateur de Ca et Kh, plus on va ajouter de produits et donc plus l'effet sera prononcé.
), en vue simplifiée, chaque molécule de carbonate sodium par rapport à un molécule de bicarbonate de sodium, est en manque d'un molécule de CO2 dissout dans le bac. Donc va en arrivant dans le bac chercher à absorber le CO2 dissout. C'est ça qui va aider le bac à monter en Ph. Plus le bac est consommateur de Ca et Kh, plus on va ajouter de produits et donc plus l'effet sera prononcé.
Donc en résumé le bailing base carbonate est un cran mieux que le bailing classique ou le RAC pour un bac à tendance "ph bas"
Hydroxyde de calcium:
L'hydroxyde de calcium, est encore un cran plus haut de ce point de vue:
un molécule d'ion hydroxyde a besoin de deux molécules de CO2 pour ressembler à ce que le bailing classique ou le RAC apportent au bac.
Donc l'hydroxyde a une influence plus forte sur le Ph du bac.
L'hydroxyde utilisé en eau de chaux, est très limitée et ne peut répondre entièrement au besoin d'un bac à haute consommation. Par contre en lait de chaux (méthode Regis Doutres), si. Mais c'est une méthode sensible à maîtriser.
http://www.cap-recifal.com/articles.htm ... chaux-r41/
Je ne suis pas en train de dire qu'il faut utiliser le bailing base carbonate ou l'hydroxyde plutôt que le RAc ou le bailing classique.
Mais juste que en fonction du ph du bac, ce choix peut se décider différemment.
Je vais peut être faire un article un jour sur la comparaison des différents méthodes de complémentation de Ca et Kh.
dans le cadre de cette discussion il y a deux aspects de cette comparaison que je voudrais expliquer:
1- Apport d'autres éléments de Ca et Kh:
Des méthodes comme le RAC, en fonction du granulat qu'on met dans le RAC, va apporter potentiellement, en plus de Ca et Kh, d'autres macro et micro éléments comme Mg, et tous les oligos éléments. Typiquement quand on met de l'aragonite qui est du squelette de corail broyé, on redissout du squelette de corail donc on va apporter à peu près tout ce que la pousse des coraux consomme.
Ceci est un peu moins vrai pour les méthodes bailing qui respectent bien l'équilibre ionique de l'eau mais qui ne vont apporter potentiellement tout le Mg et oligos que les coraux ont consommés.
Et enfin, dans les méthodes basée sur l'hydroxyde de calcium, ceci est complètement réduit à zéro: l'hydroxyde de calcium n'apporte que du Ca et du Kh (en devenir). Et donc rien d'autre. Pas de Mg, strontium, oligos,...
2- Influence sur le Ph:
chacun de ces méthodes de complémentation va influencer plus ou moins le Ph et sachant l'importance du Ph dans la pousse des coraux, suivant comment le bac se comporte en ph, ce point peut être un élément de décision important pour savoir quelle méthode de complémentation choisir:
Un bac surpeuplé où on est obligé d'avoir recours à une source de carbone pour contrôler les nitrates et phosphates, aura tendance à avoir un ph trop bas. Et donc une méthode de complémentation qui monte le ph sera plus adaptée.
Maintenant comparons les différentes méthodes de complémentation de ce point de vue:
RAC:
Le RAc, bien dimensionné et bien réglé, va rejeter peu de CO2 dans le bac. Donc si on utilise bien le RAC, le RAC est neutre point de vue Ph.
Bailing classique:
Le Bailing classique à base de bicarbonate de sodium est aussi neutre point de vue Ph. Donc disons que c'est légèrement mieux que le RAC mais la différence est faible dans le cas d'un RAC bien dimensionné et bien réglé.
Bailing base carbonate:
Le Bailing base carbonate, remplace le bicarbonate de sodium par du carbonate de sodium.
Pour pas rentrer dans des formules chimiques (ça me démange!
 ), en vue simplifiée, chaque molécule de carbonate sodium par rapport à un molécule de bicarbonate de sodium, est en manque d'un molécule de CO2 dissout dans le bac. Donc va en arrivant dans le bac chercher à absorber le CO2 dissout. C'est ça qui va aider le bac à monter en Ph. Plus le bac est consommateur de Ca et Kh, plus on va ajouter de produits et donc plus l'effet sera prononcé.
), en vue simplifiée, chaque molécule de carbonate sodium par rapport à un molécule de bicarbonate de sodium, est en manque d'un molécule de CO2 dissout dans le bac. Donc va en arrivant dans le bac chercher à absorber le CO2 dissout. C'est ça qui va aider le bac à monter en Ph. Plus le bac est consommateur de Ca et Kh, plus on va ajouter de produits et donc plus l'effet sera prononcé.Donc en résumé le bailing base carbonate est un cran mieux que le bailing classique ou le RAC pour un bac à tendance "ph bas"
Hydroxyde de calcium:
L'hydroxyde de calcium, est encore un cran plus haut de ce point de vue:
un molécule d'ion hydroxyde a besoin de deux molécules de CO2 pour ressembler à ce que le bailing classique ou le RAC apportent au bac.
Donc l'hydroxyde a une influence plus forte sur le Ph du bac.
L'hydroxyde utilisé en eau de chaux, est très limitée et ne peut répondre entièrement au besoin d'un bac à haute consommation. Par contre en lait de chaux (méthode Regis Doutres), si. Mais c'est une méthode sensible à maîtriser.
http://www.cap-recifal.com/articles.htm ... chaux-r41/
Je ne suis pas en train de dire qu'il faut utiliser le bailing base carbonate ou l'hydroxyde plutôt que le RAc ou le bailing classique.
Mais juste que en fonction du ph du bac, ce choix peut se décider différemment.
- houms

- Messages: 2650
- Âge: 55 ans
- Enregistré le: 03/07/2012
- volume du bac: 770
- mise en eau: 03/2012
- maintenance: berlinois
- éclairage: LED Vertex
- mon bac: post266343.html#p266343
Re: Compléments Balling + RAC
Et plus directement en rapport avec la discussion: de mon point de vue, rien n’empêche de mixer plusieurs de ces méthodes.
soit pour sécuriser et avoir un plan B quand l'un ne marche plus, soit pour complémenter.
Par exemple: on peut utiliser de l'eau de chaux pour utiliser ce qui est possible de complémenter par cette méthode et ensuite le compléter par du bailing classique ou base carbonate.
Un autre exemple de mélange:
Comme je disais, la méthode lait de chaux, a besoin de CO2 dissout dans l'eau du bac pour transformer l'hydroxyde en KH (carbonate et bicarbonate). Du coup un bac qui consomme beaucoup peu arriver à manquer de CO2 et donc ne pas arriver à produire le Kh suffisant par la méthode lait de chaux par manque de CO2.
Dans ce cas, le complémenter un un RAC qui n'a pas à couvrir tout le besoin du bac mais juste complémenter le lait de chaux, peut être une bonne idée.
Par contre qui dit deux systèmes, dit plus de complexité de mise au point et entretient.
soit pour sécuriser et avoir un plan B quand l'un ne marche plus, soit pour complémenter.
Par exemple: on peut utiliser de l'eau de chaux pour utiliser ce qui est possible de complémenter par cette méthode et ensuite le compléter par du bailing classique ou base carbonate.
Un autre exemple de mélange:
Comme je disais, la méthode lait de chaux, a besoin de CO2 dissout dans l'eau du bac pour transformer l'hydroxyde en KH (carbonate et bicarbonate). Du coup un bac qui consomme beaucoup peu arriver à manquer de CO2 et donc ne pas arriver à produire le Kh suffisant par la méthode lait de chaux par manque de CO2.
Dans ce cas, le complémenter un un RAC qui n'a pas à couvrir tout le besoin du bac mais juste complémenter le lait de chaux, peut être une bonne idée.
Par contre qui dit deux systèmes, dit plus de complexité de mise au point et entretient.
- houms

- Messages: 2650
- Âge: 55 ans
- Enregistré le: 03/07/2012
- volume du bac: 770
- mise en eau: 03/2012
- maintenance: berlinois
- éclairage: LED Vertex
- mon bac: post266343.html#p266343
Re: Compléments Balling + RAC

houms a écrit:Le RAc, bien dimensionné et bien réglé, va rejeter peu de CO2 dans le bac. Donc si on utilise bien le RAC, le RAC est neutre point de vue Ph.
 enfin presque.
enfin presque.Dans le RAC le CO2 sert à 2 choses
1) former des carbonates : c'est la partie utile
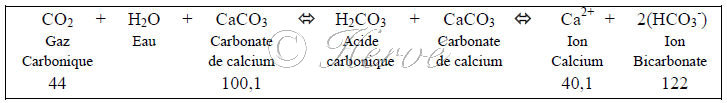
2) acidifier l'eau pour qu'elle dissolve le substrat : c'est la partie inutile mais nécessaire;
l'eau qui sort du RAC emporte une partie de CO2 qui va acidifier le bac, on ne peut pas faire autrement, il n'est donc pas correct d'écrire "le RAC est neutre point de vue Ph", mais ce qu'on peut dire c'est qu'un RAC "bien dimensionné et bien réglé" acidifie peu le bac, c'est la raison pour laquelle il faut bien choisir la taille RAC en fonction du volume du bac et de sa consommation KH et régler le débit d'eau du RAC en fonction de son volume et du type de substrat afin qu'il exporte dans le bac le strict nécessaire à son fonctionnement.
Tout ceci est expliqué ici http://www.rudyv.be/Aquarium/Articles/RAC.pdf.
_____________________________
... ce que j'écris n'est jamais que mon avis.
... ce que j'écris n'est jamais que mon avis.
- Hervé

- Messages: 18709
- Âge: 72 ans
- Enregistré le: 21/06/2011
- Localisation: Jurbise - Belgique
- volume du bac: 750
- mise en eau: 03/07/2004
- maintenance: berlinois
- éclairage: LED DIY
18 messages
• Page 1 sur 1
Retourner vers l'eau du bac,physique,la chimie,ajout etc...
Retourner vers Index du forum
Qui est en ligne
Utilisateurs parcourant ce forum : Aucun utilisateur enregistré et 56 invités








