Voici une critique à l'encontre de l’expérimentation de Toonen et Wee (2005) citée dans le Zebra.
Critique écrite par le Pr Jaubert, non retenue par Zebra (cf plus bas):
Les commentaires qui suivent concernent l’article ci-dessus désigné, récemment publié dans ZebrasO’mag (numéro 38), dont l’auteur est Nicolas Leclerc.
Cet article, fait référence aux résultats et conclusions d’articles publiés il y a une dizaine d’année par deux scientifiques américains de l’Université de Hawaii (Toonen et Wee : 2005a, b & c).
I - Premier commentaire
En premier lieu, j’ai le regret de devoir signaler que Nicolas Leclerc commet deux erreurs flagrantes.
La première erreur concerne le volume des bacs utilisés par Toonen et Wee. En effet, comme on peut aisément le vérifier dans les textes de Toonen et Wee (http://www.recif-france.com/Articles/Toonen/dsb.php ou http://www.advancedaquarist.com/2005/6/aafeature) leur volume hors tout était de 13,77 litres (27cm x 17cm x 30cm) et non pas de 20 litres comme l'a écrit Nicolas Leclercq. Et les conséquences de cette erreur sont loin d’être négligeables. En effet, c’est à partir de ce volume et surtout de la hauteur d’eau libre que l’on peut calculer le volume moyen d’eau libre qui intervient dans le calcul du taux de brassage, lequel, comme on le verra plus loin, joue un rôle fondamental. Les photos des aquariums expérimentaux, publiées par Toonen et Wee, permettent d’estimer que la hauteur d’eau libre était d’environ 17 cm, ce qui donne un volume d’eau libre de : 7,8 litres (27cm x 17cm x 17cm). On est loin des 20 litres indiqués par Nicolas Leclerc.

La deuxième erreur, aussi flagrante que la première, concerne le débit des pompes et donc le taux de brassage. En effet, comme cela est indiqué dans leurs articles, précédemment cités, Toonen et Wee précisent que le débit des pompes qu’ils ont utilisées était d’environ 189 litres par heure. Or, dans un volume d’eau de 7,8 litres, un tel débit provoque un brassage de 23,2 fois le volume par heure (184 : 7,8 = 23,2) soit plus de 2 fois plus que les 10 litres mentionnés par Nicolas Leclerc.
Nicolas Leclercq aurait dû se limiter à résumer le contenu de publications scientifiques réputées exactes en se gardant de toute interprétation. Mais, il ne l’a pas fait.
Nicolas Leclercq est un des anciens doctorants qui ont préparé leur thèse dans mes laboratoires et dont j'ai suivi les travaux. Il est l'auteur de plusieurs articles scientifiques dont je suis co-auteur. Aussi, suis-je très surpris (l’expression est faible) qu’il ait pu commettre de telles bévues. La méthode "Jaubert" a souvent été mise en cause par le passé. Aussi est-on fondé à supposer que cette exhumation biaisée de données, vieilles de 10 ans, puisse peut-être cacher une nouvelle tentative de la discréditer.
II - Deuxième commentaire
En second lieu, je considère que Toonen et Wee ont tiré des conclusions complètement erronées des résultats qu’ils ont obtenus au cours des expériences exposées dans leurs articles (2005a, b & c).
Pourquoi ?
Tout simplement parce que ces deux auteurs ont utilisé un protocole expérimental totalement inadéquat. En effet, avec un brassage horaire d’environ 23 fois le volume d’eau libre, la percolation (forçage d’eau à travers le sédiment) induite par le phénomène d’advection* était très intense. De ce fait, quelle que soit leurs épaisseurs et leurs granulométries, les sédiments testés ne pouvaient pas comporter de zones suffisamment hypoxiques pour que la dénitrification puisse s'accomplir. Pire, des sédiments percolés avec une telle intensité par de l’eau riche en oxygène deviennent des filtres sous sable et donc de véritables usines à fabriquer des nitrates. C’est la raison pour laquelle, à la fin de leur manip (au bout de 111 jours), Toonen et Wee ont trouvé, dans tous leurs bacs, avec ou sans plénum et quelle que soit l’épaisseur et la granulométrie des sédiments qu’ils contenaient, des concentrations de nitrates énormes de l’ordre de 60 à 100 mg par litre (graphique ci-dessous).
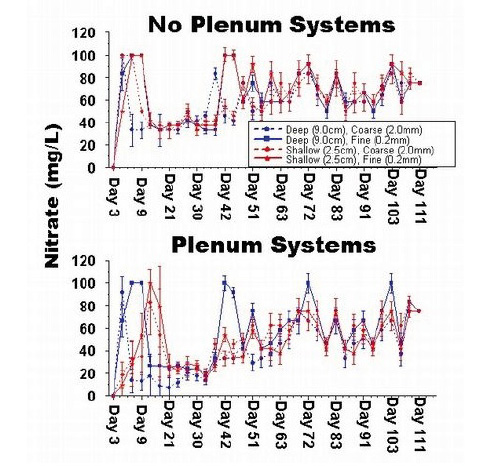
*L’advection est un phénomène bien connu, décrit pour la première fois par Huettel et al. (1996).
Certes, au moins l’un des 3 articles de Toonen et Wee, cités en référence, a été publié dans Aquaculture qui est une revue scientifique internationale à comité de lecture. Certes, dans ce genre de revue, les articles sont expertisés par des référés. Ils sont donc réputés exacts. Cependant, il arrive parfois (et ce n'est pas rarissime) que des référés laissent passer des erreurs qu'ils n'ont pas détectées. Et, de toute évidence, c'est ce qui s'est produit.
III - Troisième commentaire
Par ailleurs, je crois opportun de rappeler que les dispositifs, avec ou sans plénum, ne sont que deux façons très proches de mettre en oeuvre le principe (dénitrification biologique dans les zones hypoxiques des sédiments) : (a) dont que j'ai découvert l’existence en 1979 ; (b) que j’ai appliqué, pour la première fois dans le monde, pour équilibrer écologiquement un aquarium récifal ; et (c) dont j'ai publié les premiers résultats, il y a 35 ans, dans la revue Vie Marine (Jaubert, 1981).
L’aquarium décrit dans mes articles fondateurs (Jaubert 1981 et 1988-89) était un aquarium, qui fonctionnait depuis plusieurs années, dont j’avais simplement débranché le filtre sous sable. De ce fait, il avait hérité d’un plénum que je n’aurais pas conservé si j’avais installé un nouvel aquarium. Certes, les aquariums équipés d’un lit de sable grossier et d’un plénum sont ceux que j’ai le plus souvent utilisés. Certes, les modalités de mise en œuvre du procédé que j’ai décrit dans le brevet déposé en février 1988 privilégient l’emploi de plénums. Cependant, je n’ai jamais prétendu qu’un plénum était indispensable au fonctionnement de ce procédé. En outre, dans les revendications du brevet, j’ai précisé que toutes sortes de substrats poreux épais, granuleux ou fibreux, comportant une zone riche en oxygène et une zone hypoxique, pouvaient être utilisés pour épurer et équilibrer un aquarium. Et j’ai fait fonctionner, avec succès, dans des bacs sans plénum, des sables fins et des couches superposées de sables fins et grossiers (résultats non publiés). Aussi, suis-je fondé à considérer que le Deep Sand Bed de Shimek (2001) est une simple variante des modalités de mise en œuvre du système "Jaubert".
Certes, j'aurais préféré publier ces arguments, objectivement étayés, dans ZebrasO’mag. Ce magazine aurait ainsi pu faire preuve d’impartialité. Malheureusement, les demandes que j’ai faites, par courrier électronique adressé à la rédaction, n’ont pas abouti.
IV – Données expérimentales complémentaires
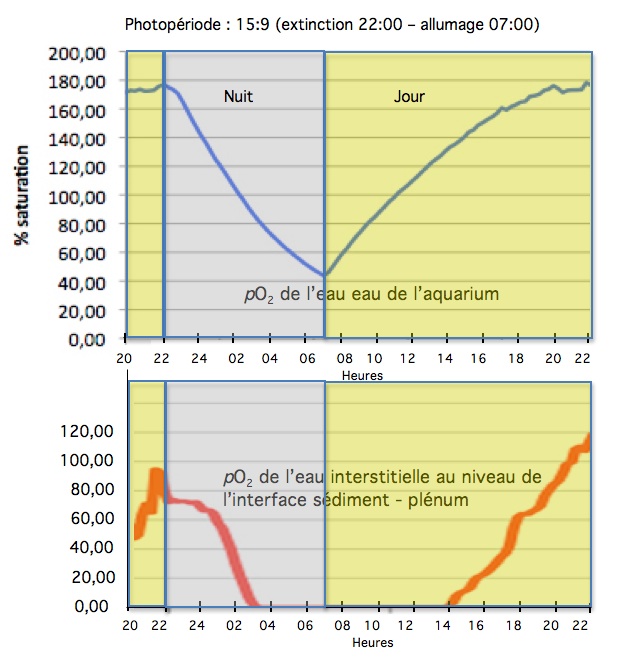
Il y a un certain temps, déjà, j’ai mesuré, dans l’un de mes nanorécifs, les variations de la concentration en oxygène (pO2) d’une part dans l’eau, et d’autre part au niveau de l’interface sédiment plénum.
Le nanorécif en question contenait une vingtaine de litres d’eau libre et son fond était recouvert d’une couche de 9 cm de sédiment corallien grossier (en moyenne 1-3mm). Le taux de brassage, produit par une petite pompe (EHEIM compact 300), bridée, était d’environ de 100 litres par heure (soit 5 fois le volume d’eau libre). La sonde était une “dipping probe”, capteur optique fabriqué par la firme allemande PRESENS. Elle était enfoncée dans le sédiment de façon que son extrémité sensible soit positionnée contre la grille qui séparait le sédiment du plénum dont l’épaisseur était d’environ 1cm. Dans cet aquarium, en fonction depuis près de 2 ans, la concentration de nitrate était inférieure à 1 mg par litre.

Ces mesures, que je n’ai pas encore publiées, montrent que les variations de la pO2 sont très importantes, dans l’eau comme dans le plénum. Dans l’eau, le maximum, en fin de journée, est de 180% de la saturation et le minimum, en fin de nuit, est de 42%. Le plénum devient hypoxique (voire anoxique) seulement 5 heures après l’extinction de l’éclairage et cette période ne dure que 11 heures. Après quoi il redevient oxique et sa pO2 peut atteindre120% de la saturation en fin de journée.
On voit donc bien qu’avec un brassage très important le plénum n’aurait jamais été hypoxique.
L’alternance de phase oxiques et hypoxique ne fait que bloquer temporairement la dénitrification hétérotrophe. En effet, les acteurs de cette dénitrification sont des bactéries anaérobiques facultatives.
Elles ne dénitrifient pas lorsqu’elles sont dans un milieu riche en oxygène, parce qu’elles métabolisent les matières organiques dont elles se nourrissent en utilisant l’oxygène dissous plutôt que celui des ions nitrate. En revanche, elles dénitrifient lorsqu’elles sont dans un milieu hypoxique, parce que la destruction des ions nitrate est le seul moyen dont elles disposent pour obtenir de l’oxygène.
Références citées
Jaubert J., 1981. Le circuit fermé marin sans filtre: premiers résultats. Vie Marine, 3: 47-52.
Jaubert, J., (1988) 1989. An integrated nitrifying-denitrifying biological system capable of purifying seawater in a closed circuit system. In: Proceedings of the second International Aquarium Congress, Monaco 22-27 février 1988. Bulletin de l’Institut Océanographique Monaco, 5 :101-106.
Huettel M., Ziebis W., Forster S., 1996. Flow-Induced Uptake of Particulate Matter in Permeable Sediments. Limnology and Oceanography, 41 (2) : 309-322.
Shimek R., 2001. Sand Bed Secrets : The common-sense way to biological filtration. Editor Marc Weiss Companies, Inc., Fort Lauderdale, Florida, USA : 36 p (ISBN: 0-9664549-6-0).
Toonen R. J., Wee C., 2005 a. An experimental comparision of sandbeds and plenum-based systems.
Part 1 : controlled lab dosing experiments. Advanced Aquarist : 4 (6).
Toonen R. J., Wee C., 2005 b. An experimental comparision of sandbeds and plenum-based systems. Part 2 : live animal experiments. Advanced Aquarist : 4 (7).
Toonen R. J., Wee C., 2005 c. An experimental comparison of sediment-based biological filtration designs for recirculating aquarium systems. Aquaculture 250 : 244-255.
Dans le post où le Pr s'exprime (et avec les photos)
http://www.lamethodejaubert.com/t2207-l ... t-de-sable